Aufgaben des Instituts
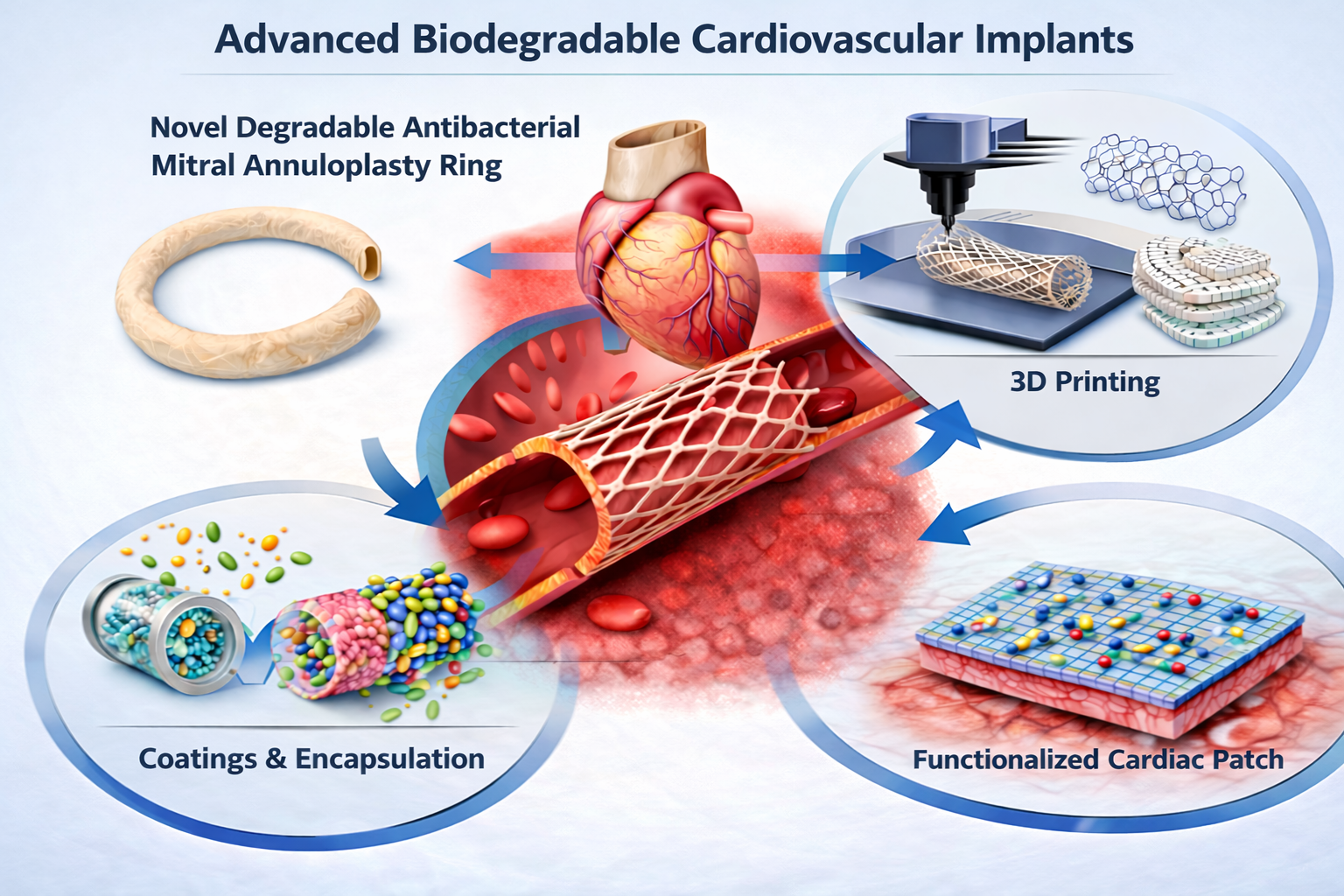
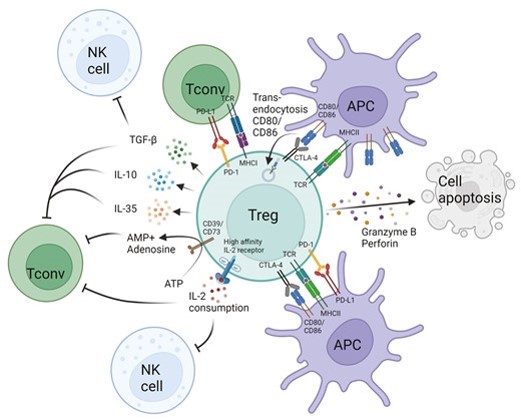
Das Institut konzentriert sich auf die Folgen von Druck- und Volumsbelastung auf das Herz und den Kreislauf (Dr. Podesser & Dr. Kiss-Lab), die Entwicklung kleinlumiger künstlicher Gefäße (Dr. Bergmeister-Lab), die Erforschung der Immunologischen Folgen der Atherosklerose (Dr. Hohensinner-Lab). Neu ist die Etablierung einer 3D Biodruck-Forschungsgruppe (Dr. Schneider) sowie der 3D-Druck von biologisch abbaubaren Polymeren (Dr. Enayati-Lab). Auf dem Gebiet der Translationalen Immunologie ist die Transplantationsimmunologie (Dr. Pilat-Lab) ein besonderer Schwerpunkt.
Herz-Kreislauf-Erkrankungen
Herzkrankheiten sind nach wie vor die Haupttodesursache in der westlichen Welt. Die Entwicklung neuer Therapien zur Behandlung von geschädigtem Herzgewebe ist von entscheidendem klinischen und wissenschaftlichen Interesse. Mit 38,6 % der Fälle waren Herz-Kreislauf-Erkrankungen die häufigste Todesursache der österreichischen Bevölkerung im Jahr 20191. Die wichtigsten Risikofaktoren sind arterielle Hypertonie, Hypercholesterinämie, Rauchen, Übergewicht, körperliche Inaktivität, sozialer Stress und genetische Faktoren. Um neue therapeutische Ansätze zu finden, intrazelluläre Prozesse besser zu verstehen und wirksamere Behandlungsmethoden zu entwickeln, konzentriert sich das Zentrum für Biomedizinische Forschung gezielt auf die Herz-Kreislauf-Forschung und ist mit zwei Arbeitsgruppen auch im Ludwig Boltzmann Institut für Kardiovaskuläre Forschung integriert.
Forschungsthemen
Forschungspartner
- Zentrum für Medizinische Physik und Biomedizinische Technik
- Universitätsklinik für Plastische, Rekonstruktive und Ästhetische Chirurgie
- Universitätsklink für Chirurgie, Klinische Abteilung für Herzchirurgie
- Universitätsklink für Chirurgie, Klinische Abteilung für Thoraxchirurgie
- Zentrum für Anatomie und Zellbiologie, Abteilung für angewandte Anatomie
- Universitätsklinik für Radiologie und Nuklearmedizin
- Department für Innere Medizin, Klinische Abteilung für Kardiologie
- Universitätsklinik für Anästhesie und Allgemeine Schmerztherapie
- Universitätsklinik für Physikalische Medizin und Rehabilitation
- Universitätsklinik für Mund-, Kiefer- und Gesichtschirurgie
- Klinisches Institut für Phatologie
- Core Facilities
- Universitätsklinik für Gastroenterologie