Vor der Implantation müssen die Biokompatibilität, die immunmodulatorischen Eigenschaften und die Funktionalität eines Implantats gründlich getestet werden. Ein breites Spektrum modernster In-vitro-Biomaterial-Bewertungsinstrumente ermöglicht einen besseren Einblick in die Interaktion zwischen Wirt und Biomaterial.
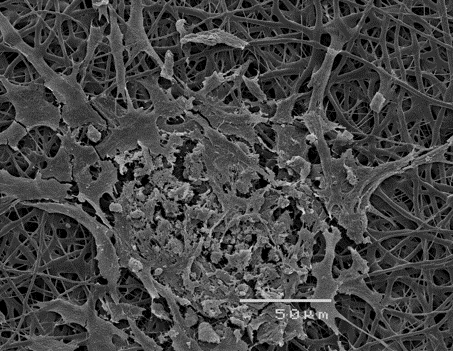
Unser Ziel ist die Entwicklung prädiktiver zellbasierter Modelle, um die Immunantwort und den biologischen Abbau in den Patienten bzw. in der Patientin abschätzen zu können. Zu diesem Zweck entwickeln wir verschiedene in-vitro-Modelle in Mono- und Co-Zellkulturen. Die Auswahl der Zelltypen in den Co-Kulturen richtet sich nach der Anwendung und dem Ort der Implantation. Darüber hinaus untersuchen wir innovative Perfusions-Bioreaktorsysteme für Zellbesiedelungszwecke, die gemeinsam mit dem Zentrum für Biomedizinische Physik und Biomedizinische Technik der MedUni Wien (H. Schima) entwickelt werden.
Laufende Projekte

Die Bewertung der Biokompatibilität und der immunmodulatorischen Eigenschaften eines Implantats ist ein entscheidender Schritt bei der In-vitro-Charakterisierung eines Biomaterials. Herkömmlicherweise wird bei dieser Bewertung nur ein Zelltyp, vor allem Makrophagen, verwendet. In diesem Projekt verfolgen wir einen spannenden Ansatz, indem wir ein Co-Kultur-Modell als Instrument zur Bewertung der Biokompatibilität von Biomaterialien entwickeln. Die Auswahl des Zelltyps in der Co-Kultur basiert auf der Anwendung und dem Ort der Implantation. Nach der Implantation eines Gefäßersatzmaterials sind Makrophagen und Fibroblasten die beiden wichtigsten Zelltypen, die an der Schnittstelle zwischen PatientIn und Biomaterial rekrutiert werden. Daher werden Makrophagen- und Fibroblasten-Mono- und Co-Kulturen in parakriner und juxtakriner Anordnung verwendet, um die Gefäßimplantate zu bewerten. Die Co-Kultur-Modelle zeigen eine höhere Übereinstimmung mit dem immunmodulatorischen/biokompatiblen Verhalten des Implantates in vivo.
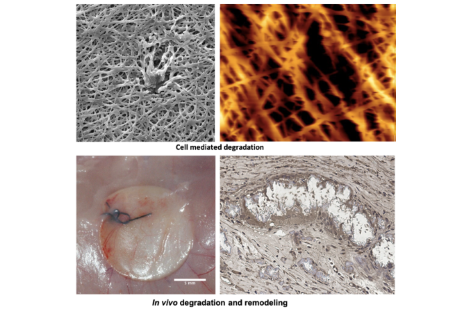
Ein zuverlässiges Bewertungsinstrument zur Beurteilung des Abbaus biologisch abbaubarer Materialien in einer annähernd physiologischen Umgebung wird noch benötigt. Die meisten der bisherigen In-vitro-Studien zum Polymerabbau wurden in nicht-physiologischen Umgebungen durchgeführt, z.B. in Gegenwart von phosphatgepufferter Kochsalzlösung, enzymatischen, oxidativen Lösungen oder bei erhöhter Temperatur (150 °C). Da Makrophagen eine entscheidende Rolle beim Abbau spielen, wurde ein Zellkulturmodell mit primären Monozyten-Makrophagen entwickelt, um den Abbau von Gefäßimplantaten über einen längeren Zeitraum in vitro zu untersuchen. Um den Untersuchungszeitraum zu verlängern, wird in diesem Projekt die Technik der Wiederaussaat angewandt. Die Kultur primärer Zellen ist in der Lage, die Zellverarbeitung in Echtzeit nachzuahmen und eine individuelle Reaktion zu zeigen. Dieses Instrument könnte für biologisch abbaubare Biomaterialien in der regenerativen Medizin eingesetzt werden.

